- Generalidades del TAB en el embarazo
Anteriormente se consideraba que el embarazo era un factor protector frente a la enfermedad mental, ahora se sabe que el embarazo es un período en el que aumenta el riesgo de recaída. El TAB es una patología que generalmente inicia en la edad reproductiva femenina (adolescencia, adultez temprana) y que aún con manejo farmacológico, se asocia a pobres desenlaces en el embarazo como mayor número de cesáreas, parto pretérmino, microcefalia e hipoglicemia.
Existen dos posibles escenarios, una paciente sin diagnóstico de TAB que debuta durante el embarazo o el posparto inmediato o una paciente diagnosticada que se embaraza.
En el primer escenario, dentro de los trastornos del ánimo en el embarazo y posparto sobresale el TAB; las pacientes que debutan en este período tienen mayor riesgo de recurrencia, suicidio e infanticidio. Generalmente definen psicosis posnatal como la presencia de síntomas psicóticos (alucinaciones, trastornos del pensamiento y comportamiento desorganizado) en los tres meses posparto, pero el período más común de aparición de estos síntomas se encuentra entre las primeras 48-72 horas y las siguientes 2 a 4 semanas.
Epidemiológicamente, las mujeres tienen una probabilidad mayor de ser admitidas en una unidad psiquiátrica en el período posparto que en cualquier otro período en sus vidas. La incidencia es de 1-2/1000 partos, siendo el riesgo entre el 25 y el 50% en pacientes con antecedente de TAB y del 57% en pacientes con antecedentes de una psicosis posparto. Los episodios psicóticos posparto por esquizofrenia son raros, con un RR <1 mientras que el de las psicosis afectivas es de 22 y el riesgo de suicidio en pacientes que experimentaron psicosis posparto es del 4%.
Algunos Factores de riesgo para psicosis posparto identificados son la primiparidad, alteraciones en el sueño, parto por cesárea, bajo nivel socioeconómico, complicaciones durante el parto, parto pretérmino, bajo peso al nacer y muerte neonatal. Mientras que la depresión posparto comúnmente se asocia a factores psicosociales, la psicosis posparto se asocia más a factores biológicos.

Los síntomas más comunes en la psicosis posparto son los maníacos, estos son de inicio súbito, generalmente entre las 48 horas y las 2 semanas posparto, progresando rápidamente hasta las alucinaciones, comportamiento desorganizado y la labilidad emocional. Generalmente son crisis graves que requieren hospitalización.
Se han diseñado algunas medidas prenatales para favorecer la detección de pacientes con alto riesgo de enfermedad mental durante el embarazo, entre ellas el TAB. En los controles prenatales se recomienda incluir preguntas de tamiz sobre antecedente de enfermedad mental como esquizofrenia, TAB, depresión y psicosis durante embarazos previos, tratamientos previos con psiquiatría o historia familiar de enfermedades mentales. También se deben utilizar las preguntas de Whooley que interrogan sobre ánimo triste y anhedonia.
- durante el pasado mes: ¿se ha sentido desanimado/a, deprimido/a o sin esperanza?
- durante el pasado mes: ¿ha tenido poco interés o ha disfrutado poco haciendo cosas?
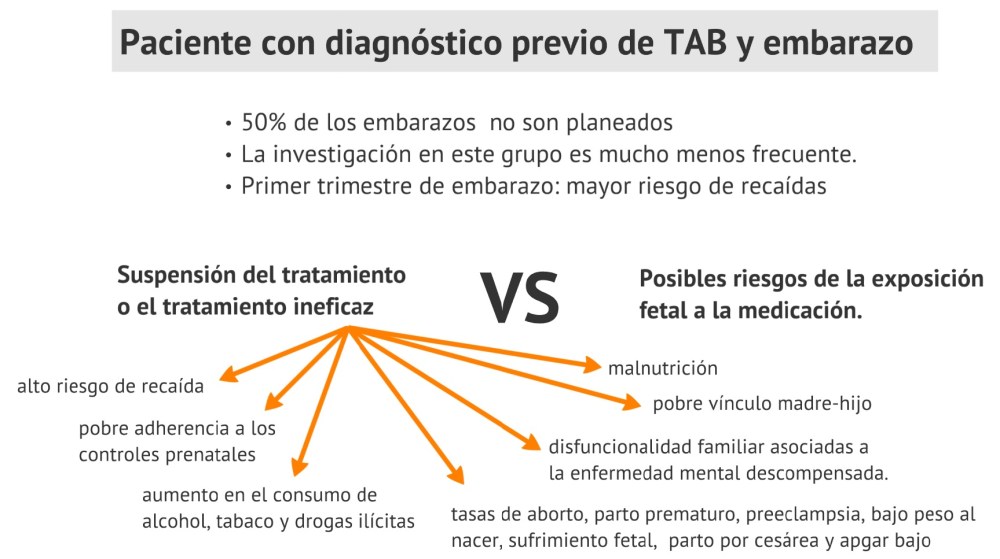
En el segundo escenario es el de la paciente diagnosticada que se embaraza. Se estima que el 50% de los embarazos en pacientes bipolares son no planeados y la investigación en este grupo es mucho menos frecuente. La evidencia ha mostrado que el primer trimestre de embarazo es el de mayor riesgo de recaídas y que la suspensión del tratamiento o el tratamiento ineficaz de los trastornos mentales durante el embarazo, puede generar mayores riesgos para la madre y su hijo en comparación a los posibles riesgos de la exposición fetal a la medicación. Son pacientes con mayores tasas de morbilidad y alto riesgo de recaída, aumento en el consumo de alcohol, tabaco y drogas ilícitas, en las tasas de aborto, parto prematuro, preeclampsia, bajo peso al nacer, sufrimiento fetal, parto por cesárea y apgar bajo. Además, también se ha reportado malnutrición, pobre adherencia a los controles prenatales, pobre vínculo madre-hijo y disfuncionalidad familiar asociadas a la enfermedad mental descompensada.
Viguera et al en el 2000 realizó un estudio en el que comparó tasas de recurrencia de 101 mujeres con TAB, unas embarazadas y otras no, luego de la descontinuación del litio. Las tasas de recurrencia fueron similares en ambos grupos (52% vs 58%) pero las recaídas en el período posparto fueron 2.9 veces más frecuentes. Posteriormente en 2007 realizó un estudio de cohortes prospectivo donde estudió a 89 pacientes embarazadas que continuaron o suspendieron el tratamiento durante la gestación y encontró que el riesgo de al menos una recurrencia durante el embarazo fue del 71%, con predominio de los episodios depresivos o con síntomas mixtos (74%) y el 47% sucedieron en el primer trimestre. Específicamente para las que suspendieron el tratamiento, el riesgo de recurrencia fue el doble, el tiempo para presentar la recurrencia fue 4 veces menor y el tiempo en crisis fue 5 veces el de las pacientes que continuaron tratamiento.
En 2012, Boden et al investigaron los riesgos de desenlaces adversos del embarazo y parto (parto pretérmino, alteraciones en el peso al nacimiento, diabetes gestacional, morbilidad neonatal y malformaciones congénitas) en 332137 pacientes embarazadas, algunas con TAB y de estas, con y sin tratamiento, entre el 2005 y el 2009.
Los resultados mostraron un aumento en el riesgo de parto pretérmino del 50% en tratadas y no tratadas, en las no tratadas hubo 3.9% de microcefalia comparado con 2.3% de la población sin TAB, y la tendencia fue similar en alteraciones del peso al nacer, en las no tratadas hubo hipoglicemia neonatal en 4.3% comparado con 2.5% de la población sin TAB y 3.4% de las pacientes con TAB en tratamiento. No lograron establecer diferencias significativas y concluyeron que independiente de si se tratan o no, el TAB se relaciona con peores desenlaces del embarazo.
En conclusión, el tratamiento del TAB durante el embarazo no mejora los desenlaces del embarazo pero dejar el tratamiento si empeora estos desenlaces tanto para la madre como para el bebé. NO tratar puede ser una opción, pero la tendencia en los estudios es que sin tratamiento los desenlaces negativos son más frecuentes para el bebé.
- Tratamiento del TAB durante el embarazo
Preconcepción: las mujeres con TAB que deseen quedar en embarazo deben llevar al menos 6 meses estables, pues algunos estudios muestran menor riesgo de recaída durante el embarazo si el periodo asintomático previo al embarazo es largo, aunque no hay una duración mínima establecida. Durante el período preconcepcional se debe explicar a la paciente los riesgos y beneficios del uso de estabilizadores tanto antenatales como durante el embarazo y con base en ello, decidir si definitivamente se quiere embarazar y si va a recibir o no medicamentos durante el embarazo. En caso de que la paciente decide suspender el tratamiento, se debe hacer un desmonte gradual a lo largo de 2-4 semanas con monitoreo sintomático. Este monitoreo incluye el automonitoreo de la paciente para lo cual debe recibir psicoeducación sobre su enfermedad y los síntomas.
Todos estos medicamentos atraviesan la placenta, aunque en grado variable. Los de mayor riesgo identificado son los antiepilépticos por su relación con defectos del tubo neural.
Se recomienda una dosis de 4mg de ácido fólico/día un mes antes de la concepción, pues si bien no hay estudios que demuestren que disminuyen los efectos teratogénicos sobre el tubo neural en pacientes que reciben antiepilépticos, si hay estudios que demuestran que disminuye estos defectos en población general. Si la paciente viene con Valproato o carbamazepina, se deben cambiar por otro haciendo un switch gradual (no se recomienda suspensión abrupta).
Se debe tener en cuenta que los antipsicóticos de segunda generación pueden producir hiperprolactinemia como efecto secundario, lo cual disminuye la posibilidad de quedar en embarazo.
Finalmente hay mejores resultados cuando psiquiatra y ginecólogo trabajan juntos con mejores resultados en salud mental para la madre y el neurodesarrollo del feto.
TAB no tratado:
- Una paciente con TAB en embarazo y sin tratamiento o que lo suspende tiene un mayor riesgo de recaída y un mayor tiempo de recuperación, además la tasa de recaída en el posparto en pacientes sin tratamiento o tratamiento suspendido es 3 veces mayor.
- Aumenta el riesgo del embarazo por exposición a cigarrillo, alcohol y otras sustancias.
- Aumenta el riesgo de desenlaces adversos del embarazo y en el neurodesarrollo del feto (afecta función motora, inteligencia y desempeño social). El TAB por si solo se relaciona con microcefalia, feto pequeño para la edad estacional, prematuridad, apgar bajo al nacer e ingreso a UCI neonatal.
- En el período perinatal, aumenta el riesgo de pobres cuidados para el bebé con alteración en la formación del vínculo madre-hijo, de suicidio durante el primer año posparto (el suicidio es una de las causas frecuentes de muerte en el embarazo) y de infanticidio.
Manejo del TAB durante el embarazo
- Se realiza mediante una aproximación caso por caso, individualizada.
- Confirmar diagnóstico de TAB.
- Intentar monoterapia. Se considera de menor riesgo la exposición fetal a una dosis alta de un medicamento que una exposición a múltiples fármacos a dosis bajas.
- No se recomienda el uso de antidepresivos en monoterapia por aumento en el riesgo de recaída.
- Los estudios demuestran una mayor tasa de recaídas cuando se suspenden los estabilizadores durante el embarazo y las recaídas son más frecuentes en el grupo que los suspende cuando lo hacen de forma abrupta.
- Antecedente de ciclaje rápido es un factor de riesgo para recaída durante el embarazo, otros factores que influyen son la severidad de los episodios previos, el fácil acceso al psiquiatra y la presencia de una red de apoyo adecuada.
En general, hay 4 posibles opciones de tratamiento del TAB durante el embarazo:
- En el caso de una enfermedad estable con factores protectores (acceso fácil al psiquiatra, buena red de apoyo, antecedente de buena respuesta al tratamiento farmacológico): La opción más segura es desmontar gradualmente el tratamiento y vigilar síntomas mientras la madre recibe psicoterapia, lo que podría disminuir el riesgo de recaída en teoría (no hay evidencia).
- Seleccionar un psicofármaco y desmontar los otros. No se recomienda dejar únicamente un antidepresivo como monoterapia porque aumenta el riesgo de recaída. En caso de decidir utilizarlo, debe ser siempre acompañado de un estabilizador del ánimo.
- Suspender el tratamiento durante el primer trimestre (organogénesis, mayor riesgo de teratogenicidad) y reiniciarlo durante el segundo y tercer trimestre. La suspensión durante el embarazo debe ser gradual, pues los estudios demuestran que la suspensión abrupta aumenta el riesgo de recaída. Los más recomendados son el litio, la lamotrigina o los antipsicóticos de primera y segunda generación.
- Cambio de medicamento hacia uno con mejor perfil para el feto.
Fármacos
El medicamento más estudiado para manejo del TAB en embarazo es el litio y se ha demostrado que disminuye el riesgo de recaídas durante el embarazo y el posparto.
Siempre se deben considerar dos potenciales confusores en estos casos, como son la tasa basal de malformaciones en las maternas (entre 2 y 4%) y que el trastorno como tal podría ser teratogénico. El litio se ha asociado a teratogenicidad cardíaca, específicamente a cardiopatía de Ebstein (implantación baja de las valvas septal y posterior de la válvula tricúspide). En los primeros estudios de litio, se documentó una prevalencia de 400 veces la de la población normal, posteriormente se encontró una de 20 veces la de la población normal y en los estudios de litio más recientes reportan prevalencias escasamente superiores en las pacientes que toman litio.
Un estudio gigante de 2017 hecho por Patorno et al incluyó 1.3 millones de embarazos, 663 de ellos con exposición al litio, mostró una tasa de malformaciones cardiacas fue de 2.41% en expuestos vs 1.15% en no expuestos, con un riesgo ajustado de 1.65 para los expuestos a dosis de 600mg/día (IC 95%, 0.67 – 3.8) y de 3.22 (IC 95%, 1.47 – 7.02) para los expuestos a dosis de 900mg/día o más.
De los pacientes con cardiopatía, la prevalencia de anomalía de Ebstein en exposición a litio fue 0.6 vs 0.18 en los no expuestos con cardiopatía, con un riesgo ajustado de 2.66 (IC95%, 1 – 7.06)
Generalmente se debe aumentar la dosis de litio en el segundo y tercer trimestre del embarazo por los cambios fisiológicos normales de este estado (aumento del volumen circulante, aumento en la TFG) lo que lleva a un aumento del 30 a 50% en la eliminación del fármaco
Debe realizarse monitoreo mensual con litemia, TSH y creatinina hasta la semana 36, de ahí en adelante semanal hasta el parto. Sugieren una ecografía de segundo nivel al inicio del segundo trimestre como tamiz de posibles malformaciones en el feto.
En el posparto se debe continuar el litio a las dosis a las que venía previo al embarazo con especial cuidado en la hidratación de la paciente para evitar intoxicaciones por deshidratación.
El litio en la lactancia sigue siendo controversial, en los últimos años se apoya la lactancia materna a pesar de que se sabe que el litio tiene niveles importantes e leche materna siempre y cuando se cuente con un pediatra en el equipo que monitorice creatinina y TSH en el neonato.
- Valproato de sodio: Muy teratogénico (5-9%), definitivamente proscrito durante el primer trimestre, pero es permitido durante la lactancia. Una revisión de Cochrane de 2014 encontró que los niños con exposición a Valproato in útero tienen menor IQ, sin embargo esta revisión fue realizada con madres que sufrían epilepsia, no TAB.
- Carbamazepina: mayor riesgo de espina bífida (26/10.000) y otras alteraciones del tubo neural, hernia diafragmática, anomalías esqueléticas e hipospadia además de parto pretérmino y bajo peso al nacer, la mayoría de estos hallazgos han sido con dosis >1gr/día. Este medicamento induce los anticonceptivos orales.
- Lamotrigina: Algunos estudios sugieren asociación con paladar hendido, pero los más recientes no han logrado demostrar dicha asociación, por lo que se considera un agente con perfil benigno con tasas de malformaciones similares a las de la población general (2-5%). Se debe vigilar en el tiempo cercano al parto por un aumento en su clareance debido a que los estrógenos inducen la glucuronidación.
- Antipsicóticos de primera generación: están mínimamente asociados a malformaciones pero se ha reportado parto pretérmino, síntomas extrapiramidales, inquietud, temblor, hipertonía, distonía y abstinencia con ellos. Se han reportado casos de parkinsonismo en neonatos expuestos in útero a haloperidol, pero se desconoce su relevancia clínica ya que fueron de corta duración (2-6 días)
- Antipsicóticos de segunda generación: La asociación con alteraciones durante el embarazo es muy baja, pero si aumentan el riesgo de diabetes gestacional, hipertensión, obesidad y síndrome metabólico. Las guías NICE recomiendan el uso de estos medicamentos antes que el del litio en pacientes con TAB previo al embarazo o durante el mismo.
Dos de los más estudiados son la olanzapina y la quetiapina, esta última parece ser la opción más segura pues atraviesa en menor proporción la barrera placentaria y tiene menores efectos metabólicos que la olanzapina.
Últimamente se ha asociado la risperidona con mayores efectos teratogénicos que los otros antipsicóticos atípicos, hay algunos estudios recientes en ratones que muestran un efecto neurotóxico en el largo plazo que produce alteraciones neurocomportamentales en la adolescencia, con estudios histopatológicos donde se evidencia menor peso cerebral, disminución en el grosor de las capas neocorticales y neurodegeneración apoptótica por lo que el uso durante el embarazo no se recomienda actualmente.
- La clozapina da el doble de riesgo para el desarrollo de diabetes mellitus gestacional. Se ha asociado a síndrome del floppy baby además del riesgo de agranulocitosis en ambos. En el feto hay reportes de disminución en la variabilidad de la FCF y hay reportes de malformaciones congénitas (4.2%). Solo hay un reporte de aborto en una paciente con esquizofrenia refractaria en manejo con 75mg de clozapina/día.
- La TECAR se ha considerado una opción segura en el embarazo, pero una revisión de 2015 reporta un riesgo de complicaciones del 29% y una tasa de mortalidad fetal del 7%, lo cual va en contra de lo reportado previamente.
Los efectos secundarios más reportados de la TECAR son náusea (menos con propofol, más con ketamina), cefalea (26-85%, generalmente 2 horas posTECAR y dura alrededor de 24h pero cede con analgesia), mialgias (tienden a mejorar luego de la primera sesión) y los propios de los anestésicos (apnea prolongada, hipertermia maligna, hiperkalemia o consciencia durante el procedimiento). En el feto se ha reportado bradicardia fetal y muerte fetal y en la madre, reflujo gastroesofágico, abruptio, aborto y parto pretérmino aunque no se ha logrado establecer la relación específica entre la TECAR y dichos efectos secundarios en los estudios.
Se debe realizar en un hospital donde se cuente con los elementos para manejar las posibles complicaciones, se debe mantener informado al obstetra del caso y se debe monitorear la FCF durante la sesión.
Si durante el embarazo hay un episodio afectivo, no hay guías preestablecidas para el manejo y estos se manejan de acuerdo a las recomendaciones de las guías para TAB en pacientes que no estén en embarazo, tratando de analizar caso por caso los efectos de los medicamentos a utilizar.
En general: Valproato y carmabazepina no, quetiapina y lamotrigina son buenas opciones, el haloperidol es otra buena opción, la TECAR es otra buena opción, preferir monoterapia a polifarmacoterapia.
- Posparto
Durante este periodo el riesgo de recaída aumenta todavía más que durante el embarazo, con promedio de 3.5 veces y la mayoría de las recaídas ocurren en las primeras 4 semanas posparto.
Presentar una recaída posparto aumenta el riesgo de sufrir nuevas recaídas posparto en el futuro y entre el 72 y el 88% de los episodios psicóticos posparto son debidos al TAB.
Se recomienda suspender litio 24-48 previas al parto y una adecuada hidratación durante el mismo, otra opción es disminuir la dosis que venía recibiendo la semana previa al parto en un 25 a 50%. Las complicaciones neonatales asociadas incluyen el síndrome del floppy baby (cianosis e hipotonía), diabetes insípida nefrogénica, hipotiroidismo, hipotonía, letargo, taquicardia, cianosis y dificultad respiratoria.
La dosis de lamotrigina debe disminuirse en el posparto pues al revertir los cambios fisiológicos del embarazo, aumenta el riesgo de toxicidad del medicamento. Normalmente se evalúa eficacia mediante respuesta clínica y no mediante niveles sanguíneos.
- ¿Qué hacer durante la lactancia materna?
Se confrontan las ventajas de la lactancia materna (mejor vínculo madre – hijo, sistema inmune más robusto y mejor función gastrointestinal) contra las ventajas del tratamiento del TAB en el posparto. Las desventajas que representa la lactancia materna en las pacientes con TAB inician con la disrupción del sueño.
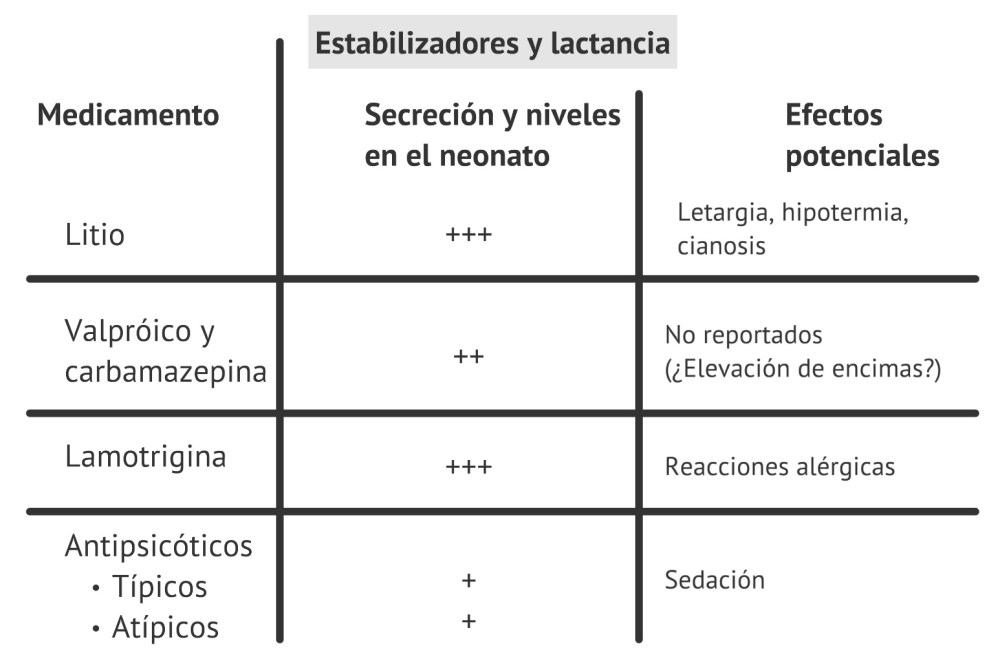
Los niveles de litio en leche materna están alrededor de la mitad del litio circulante en la madre y en el bebé, de 1/4, pero por la inmadurez renal del neonato, es importante que se vigile su estado de hidratación y se sugieren litemias periódicas, aunque no hay periodos estandarizados.
Se desconocen los efectos a largo plazo sobre el uso de litio en la lactancia materna, una opción es tomar la dosis de litio en la noche y que alguien alimente al bebé durante la noche. Durante el día, esta puede alimentar al bebé con una exposición del neonato a niveles mucho menores de litio. Cada caso de se debe individualizar pero solo se recomienda lactancia materna con litio en pacientes en las que el medicamento se haya demostrado eficaz, que tengan buena adherencia, con neonatos sin patologías comórbidas y contando con un pediatra dentro del equipo.
Esta decisión debe estar tomada mucho antes del momento del parto
El Valproato se excreta entre el 1 y 10% en leche materna y no se han reportado efectos adversos en los neonatos. Teóricamente, la inmadurez hepática del neonato haría que la vida media fuera alrededor de 47 horas, por lo que recomiendan control para trombocitopenia y hepatotoxicidad.
La lamotrigina se considera compatible con la lactancia, se excreta mínimamente en leche materna pero los bebés alcanzan a tener niveles séricos detectables. Solo hay un reporte de caso de apnea en un neonato de una madre con intoxicación por lamotrigina.
La carbamazepina se excreta por leche materna pero los niveles en los neonatos son mínimos y se considera una opción viable en lactancia.
El haloperidol se excreta por la leche materna al 3% de la dosis materna, por lo que no es contraindicación para la lactancia.
No hay estudios grandes en lactancia con los antipsicóticos de segunda generación, hay algunos con olanzapina, quetiapina y risperidona donde si bien se excretan en leche materna, los niveles son muy bajos. A pesar de ello, sugieren monitorizar al neonato por somnolencia y posibles efectos extrapiramidales.
La clozapina se excreta en leche materna y los neonatos tienen riesgo de agranulocitosis, convulsiones y sedación. La academia americana de pediatría lo clasifica como un medicamento con efecto desconocido sobre los infantes pero que podría ser de cuidado y algunos autores están en contra de su uso durante la lactancia por el riesgo de aplasia medular y que de usarse, debe realizarse HLG en el neonato semanal por seis meses.
De acuerdo con la evidencia revisada, son válidas las siguientes conclusiones:
- El TAB es una patología de muy difícil manejo durante el embarazo por el elevado riesgo de descompensación y el pronóstico de la gestación cambia radicalmente si este es producto de un proceso que inicia acompañado por el equipo de salud desde la preconcepción.
- Son pocas las certezas con los medicamentos durante el embarazo, pero en general: Valproato y carmabazepina no, quetiapina y lamotrigina son buenas opciones, el haloperidol es otra buena opción, la TECAR es otra buena opción, litio se puede usar y se debe buscar monoterapia sobre polifarmacoterapia.
- Las pacientes embarazadas con TAB son de alto riesgo obstétrico, deben tener un seguimiento estrecho por parte de psiquiatría y ginecología, especialidades que si trabajan en equipo, mejoran los desenlaces de estas gestaciones.
- Recibir tratamiento farmacológico para el TAB y la lactancia materna no son excluyentes.
Bibliografía
- Thomson, M., & Sharma, V. (2018). Weighing the Risks: the Management of Bipolar Disorder During Pregnancy. Current psychiatry reports, 20(3), 20.
- Mannion, A., & Slade, P. (2014). Psychotic-like experiences in pregnant and postpartum women without a history of psychosis. Schizophrenia research, 160(1), 118-123.
- Doucet, S., Dennis, C. L., Letourneau, N., & Blackmore, E. R. (2009). Differentiation and clinical implications of postpartum depression and postpartum psychosis. Journal of Obstetric, Gynecologic, & Neonatal Nursing, 38(3), 269-279.
- Ebeid, E., Nassif, N., & Sinha, P. (2010). Prenatal depression leading to postpartum psychosis. Journal of Obstetrics and Gynaecology, 30(5), 435-438.
- Whooley MA, Avins AL, Miranda J, Browner WS. Case-finding instruments for depression. Two questions are as good as many. J Gen Intern Med. 1997 Jul;12(7):439-45.
- Spinelli Margaret. Antidepressant Treatment During Pregnancy. Am J Psychiatry. 2012;(November):121–124.
- Bauer, M., & Gitlin, M. J. (2016). The essential guide to lithium treatment. Cham, Switzerland: Springer.
- Haskey, C., & Galbally, M. (2017). Mood stabilizers in pregnancy and child developmental outcomes: A systematic review. Australian & New Zealand Journal of Psychiatry, 51(11), 1087-1097.
- Khan, S. J., Fersh, M. E., Ernst, C., Klipstein, K., Albertini, E. S., & Lusskin, S. I. (2016). Bipolar disorder in pregnancy and postpartum: principles of management. Current psychiatry reports, 18(2), 13.
- Viguera, A. C., Nonacs, R., Cohen, L. S., Tondo, L., Murray, A., & Baldessarini, R. J. (2000). Risk of recurrence of bipolar disorder in pregnant and nonpregnant women after discontinuing lithium maintenance. American Journal of Psychiatry, 157(2), 179-184.
- Viguera, A. C., Whitfield, T., Baldessarini, R. J., Newport, D. J., Stowe, Z., Reminick, A., … & Cohen, L. S. (2007). Risk of recurrence in women with bipolar disorder during pregnancy: prospective study of mood stabilizer discontinuation. American Journal of Psychiatry, 164(12), 1817-1824.
- Bodén, R., Lundgren, M., Brandt, L., Reutfors, J., Andersen, M., & Kieler, H. (2012). Risks of adverse pregnancy and birth outcomes in women treated or not treated with mood stabilisers for bipolar disorder: population based cohort study. bmj, 345, e7085.
- Miklowitz, D. J., & Gitlin, M. J. (2014). Clinician’s Guide to Bipolar Disorder: Integrating Pharmacology and Psychotherapy. Guilford Publications.
- Patorno, E., Huybrechts, K. F., Bateman, B. T., Cohen, J. M., Desai, R. J., Mogun, H., … & Hernandez-Diaz, S. (2017). Lithium use in pregnancy and the risk of cardiac malformations. New England Journal of Medicine, 376(23), 2245-2254.
- Singh, K. P., Singh, M. K., & Singh, M. (2016). Effects of prenatal exposure to antipsychotic risperidone on developmental neurotoxicity, apoptotic neurodegeneration and neurobehavioral sequelae in rat offspring. International Journal of Developmental Neuroscience, 52, 13-23.
- Pearlstein, T. (2013). Use of psychotropic medication during pregnancy and the postpartum period. Women’s Health, 9(6), 605-615.
- Hogan, C. S., & Freeman, M. P. (2016). Adverse effects in the pharmacologic management of bipolar disorder during pregnancy. Psychiatric Clinics, 39(3), 465-475.
- Andrade, C., Arumugham, S. S., & Thirthalli, J. (2016). Adverse effects of electroconvulsive therapy. Psychiatric Clinics, 39(3), 513-530.
- Mehta, T. M., & Van Lieshout, R. J. (2017). A review of the safety of clozapine during pregnancy and lactation. Archives of women’s mental health, 20(1), 1-9.
