- Historia de la planta
El cáñamo es el nombre de una especie de plantas llamadas Cannabis. Existen tres variedades de la planta Cannabis: sativa (inicialmente africana, ahora también en Latinoamérica y el caribe), índica (Asiática) y ruderalis (norte de Europa). Fue introducida a América por los españoles, pues se utilizaban las fibras de la planta para hacer implementos de navegación como cuerdas y velas, sin embargo, los primeros en utilizarla fueron los chinos quienes además de estos implementos, fabricaban papel con el cáñamo. La primera referencia que se conoce respecto a sus propiedades psicoactivas se encuentra en el libro Atharvaveda, recopilación de cantos védicos de la India realizada entre los años 2000 y 1400 a.C. donde se refieren a ella como la hierba saha que libra de la ansiedad. En otro libro, el Zend Avesta, se denomina como vicahia y en esta descripción destacan su efecto eufórico y la capacidad para producir risa. La planta se asociaba al dios Shiva y hacía parte de su vida espiritual.
En la antigua Grecia, Herodoto hacía referencia al uso de la marihuana por parte de los escitas en sus rituales funerarios y en Roma, Galeno durante el siglo II d.C. describe su uso común en las fiestas para promover un estado de júbilo.
Durante las cruzadas, principalmente en Siria y Persia se creó una secta conformada por los nazaríes, de origen islámico chiíta. Eran conocidos como los Ḥashshāshīn, que significa “consumidor de haschis”, de esta proviene la palabra asesino. Esta secta se dedicaba a asesinatos selectivos y tácticas de espionaje y consumían marihuana por sus efectos en la toma de decisiones y control de la ansiedad.
El primer registro de la era moderna lo hizo el inglés Thomas Bowery en 1670 luego de observar los efectos de la intoxicación aguda por marihuana en sus compañeros durante un viaje a Bengala. Los clasificó en cuatro grupos: jubilosos, indiferentes, psicóticos y violentos. El uso se extendió en Europa posterior a las conquistas de Argelia y Egipto durante el siglo XIX y el consumo de marihuana se disparó entre los intelectuales parisienses como Charles Baudelaire. Posteriormente el médico Jacques Joseph Moreau escribió El Haschis y la alienación de la mente, primer compendio de psicofarmacología sobre los efectos de la planta. En Colombia hay datos sobre los cultivos de marihuana con fines textiles (ropa y costales) desde 1925 pero su uso se extendió entre las décadas de los 60’s y 70’s.
De las múltiples sustancias que contiene la planta (500 aproximadamente), las más importantes para la medicina son los cannabinoides (los hay vegetales, animales o endógenos y sintéticos), específicamente el delta 9 trans tetrahidrocanabinol responsable de los efectos psicoactivos y el cannabidiol, en estudio como posible agente terapéutico para diferentes patologías
2. Presentaciones, farmacocinética y epidemiología
Tiene múltiples nombres, a nivel internacional hablamos de mota, porro, cacho, bhang, ganja, moma, kif. En Colombia recibe otros tantos, como hierba, cilantro, turca, mariacachafa, marimba, vareta, chiruza, mona, yesca, pangola, power, crespa, join, etc. Las presentaciones pueden ser:
- Hojas, tallos y flores. (a su vez, de marihuana estándar con concentración de THC entre el 1-4%, o tipo “cripy” 5-20% )
- Resina o hachís con concentración de THC del 20%-50%
- Aceite de hachís con concentración del THC hasta del 50%-80%
Formas de consumo: en cigarrillo, pipa o pipa de agua, ingerida (4 veces menos efecto, absorción errática y más lenta por efecto de 1er paso) y frotada contra la piel.
Máximos niveles en sangre entre 7-10 minutos cuando se fuma (30-60 minutos cuando se come). Altamente lipofílica, se une 95% a proteínas y al cerebro ingresa aproximadamente el 1%, concentrándose principalmente en el tálamo, hipocampo, amígdala y corteza cerebral. El THC tiene una vida media de 4 horas pero difunde a muchos tejidos, principalmente grasos y se acumula. Es metabolizada por la isoenzima 2C19 (hidroxilación, oxidación y conjugación con glucurónido) e inhibe de manera importante la CYP2C9. La excreción se da 60% en heces y 40% vía renal.
Epidemiología

A nivel mundial, el consumo de marihuana está entre el 3.9 y el 5% con una prevalencia entre 3.8 y 3.9% en la población entre los 15 a 64 años. Para el año 2012, se calcularon 224 millones de consumidores en el mundo.
En Colombia, según el ODC (observatorio de drogas de Colombia) la marihuana es la sustancia psicoactiva ilegal más consumida en el país, seguida por la cocaína, el basuco y el éxtasis. El 87% de la población consumidora de cualquier sustancia, consume marihuana, de los cuales el 75% consume “cripy”. La población que más la consume es la escolarizada, con un promedio de inicio de consumo a los 14 años para ambos géneros.
En un estudio realizado en Colombia entre los años 2015-2016, se analizaron 316 muestras de marihuana recolectadas en 17 ciudades del país buscando la concentración de THC. Las concentraciones variaron entre 0.1% y 18.91%. El 35% de las muestras tuvieron una concentración de THC entre 5-10%, 35% entre 10-15% y el 6% entre 15-20%.
Según la ley 30 de 1986, a pesar de ser una sustancia ilegal, los colombianos pueden tener una dosis mínima que no debe exceder los 20 gramos o los 5 gramos en su presentación de hachis. En Colombia el uso medicinal está reglamentado por el decreto 2467 de 2015.
Aproximadamente el 9% de los consumidores de marihuana se volverán dependientes, porcentaje que sube a 17% si el comienzo del consumo fue en la adolescencia y a un 25-50% si además el consumo es diario. Puede desarrollar un síndrome de abstinencia leve, caracterizado por irritabilidad, dificultades al dormir, problemas con su temperamento, falta de apetito, antojos, intranquilidad y/o varias molestias físicas que se presentan más agudamente entre la primera y la segunda semana después de haber dejado de usar marihuana.
3. ¿Qué hace el THC en el cerebro?
Interactúa por medio del sistema endocannabinoide. Tiene dos receptores, ambos acoplados a proteína G: los CB1 (descubierto en 1990, distribuidos principalmente en el SNC, sobre todo en ganglios basales, capa molecular del cerebelo (conducta motora), corteza e hipocampo (memoria y aprendizaje), emociones (amígdala) y percepciones (tálamo). También se encuentran a nivel del bazo, amígdalas, corazón, próstata, útero, ovario) y los CB2 (descubierto en 1993, distribuidos en el sistema inmune, también en bazo y amígdalas, linfocitos T, B y monocitos). Los principales agonistas endocannabinoides descritos son la anandamida (descubierta en 1990, su nombre viene del sánscrito ananda, que significa “felicidad interna”, si bien después se descubrió que tiene mucha menos afinidad por el receptor CB1 que el THC y no produce la sensación de euforia o relajo de este último) y el 2-araquidonil glicerol (2-AG), los cuales están implicados en la coordinación motora, aprendizaje, memoria, antinocicepción, control de emociones, desarrollo neuronal, además de diferentes procesos a nivel cardiovascular y del sistema inmune. Los receptores CB1 inhiben la liberación de varios neurotransmisores y neuromoduladores, entre ellos la dopamina, el GABA, la serotonina, el glutamato, la noradrenalina y la acetilcolina.
Son sintetizados y liberados a partir de neuronas, son capaces de unirse y activar receptores de membrana y son inactivados por degradación enzimática, por lo que se consideran neurotransmisores. Sin embargo, no son almacenados en vesículas intracelulares, sino que se producen a partir de un precursor fosfolípido de la membrana celular.
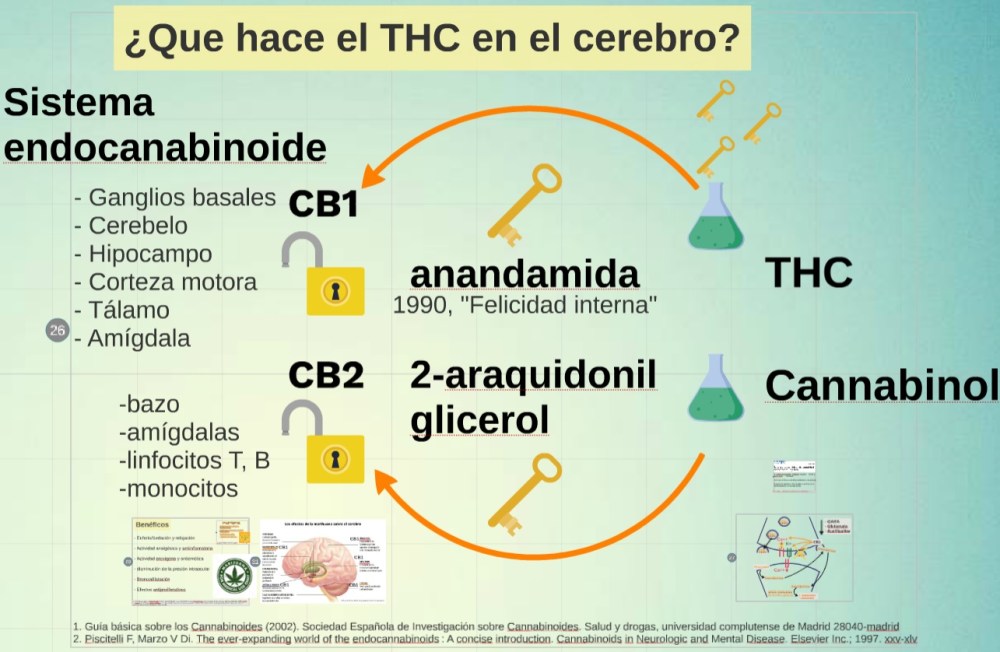
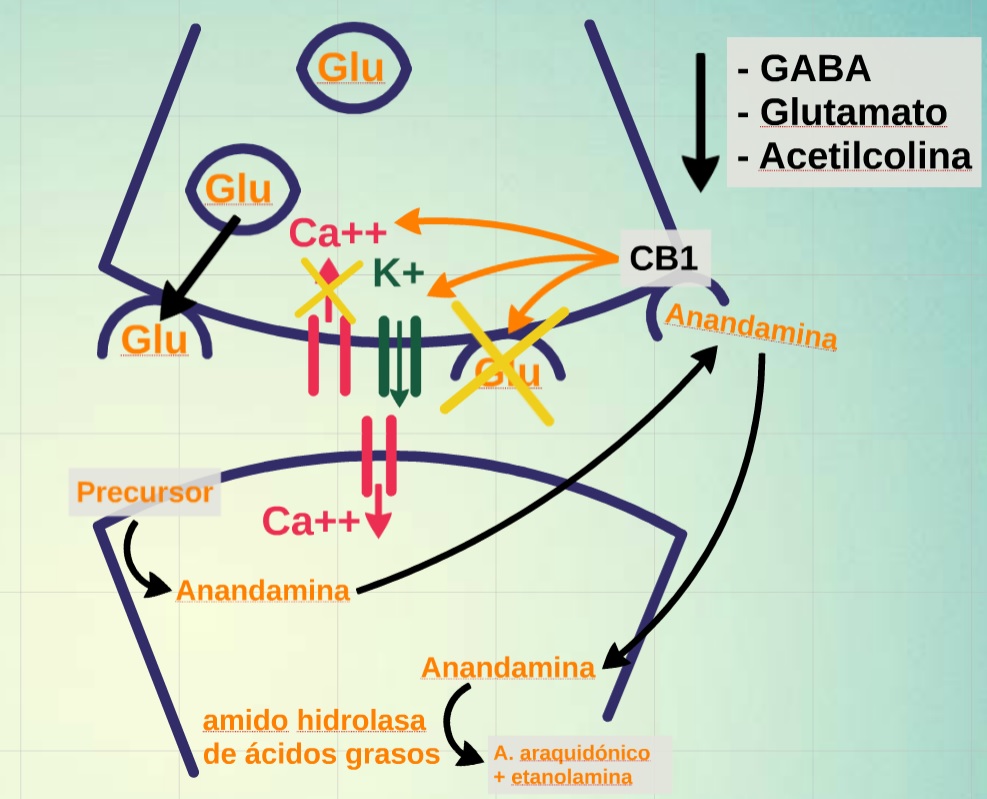
Por su gran distribución, el sistema endocannabinoide se relaciona con múltiples propiedades, por lo que estimulación mediante el uso de THC puede producir efectos benéficos y placenteros (Euforia/Sedación y relajación, Actividad analgésica y antiinflamatoria, Actividad orexígena y antiemética disminución de la presión intraocular, Broncodilatación y Efectos antiproliferativos) pero también efectos deletéreos (Ateraciones en el tono muscular y coordinación motora, Alteraciones en la percepción temporal y la memoria reciente, Hipotensión y taquicardia, Inmunosupresión a dosis altas). Su mecanismo de acción inicia cuando se ocupan y activan receptores de neurotransmisores en la membrana plasmática de una neurona postsináptica, ésta sintetiza precursores de endocannabinoides y los escinde para liberar a la hendidura sináptica endocannabinoides funcionalmente activos (anandamida y 2-AG). Esto acontece, por ejemplo, tras la unión de algunos neurotransmisores como el glutamato a sus receptores ionotrópicos o metabotrópicos. Los endocannabinoides actúan entonces como mensajeros químicos retrógrados uniéndose a receptores CB1 presinápticos, que median la inhibición de la entrada de iones Ca2+ (por cierre de canales de Ca2+ sensibles a potencial) y la facilitación de la salida de iones K+ (por apertura de canales rectificadores de K+). Ello dificulta la despolarización de la membrana y los procesos de exocitosis, bloqueándose así la liberación de neurotransmisores como glutamato, GABA o acetilcolina. La acción neuromoduladora de los endocannabinoides finaliza mediante su recaptura celular a través de sistemas de transporte de membrana y su posterior degradación intracelular por una serie de lipasas.
El sistema endocannabinoide tiene una acción en la regulación de las neuronas glutamatérgicas y GABAérgicas presinápticas, modulando la excitación e inhibición del estriado (tanto a nivel dorsal como ventral), El THC interactúa con las neuronas glutamatérgicas y GABAérgicas alterando la retroalimentación sobre las neuronas dopaminérgicas y aumentando la concentración de dopamina (DA).
Mediante estudios de RMNf y PET se han documentado además cambios a nivel del flujo sanguíneo y el metabolismo de la glucosa en circuitos dopaminérgicos frontales y subcorticales.
4. Relación entre trastornos mentales y uso de THC
Nora Volkow, directora del NIDA (National Institute on Drug Abuse) explica los efectos adversos secundarios al uso de marihuana, dividiéndolos en dos grupos: efectos a corto y a largo plazo.
Corto plazo:
Adicción: A largo plazo, el uso de marihuana puede llevar a la adicción. 9% de los que experimentan la sustancia serán adictos, aumentando a 1 de cada 6 personas si el consumo inició en la adolescencia y a 25-50% si el consumo es diario. En los últimos dos casos se asocia a que en la adolescencia el cerebro humano sufre varios cambios, incluido el sistema endocannabinoide. Adicionalmente varios estudios han demostrado que el uso diario de marihuana aumenta el riesgo de uso de otras sustancias ilícitas.
Se describen tres etapas en la adicción a sustancias:
- Intoxicación aguda: El consumo de marihuana activa el sistema de recompensa aumentando la liberación de DA y estableciendo un aprendizaje condicionado, donde la estimulación repetida hace que las neuronas no secreten DA como recompensa sino de forma anticipatoria ante las señales que se identifican antes del consumo (estar en ambientes donde se ha consumido la droga, con personas con las que se ha consumido y el estado mental en el que se consumió anteriormente). Mientras mayor sea la motivación, la persona está dispuesta a soportar más consecuencias negativas del consumo y diferente a lo que pasa con otras recompensas como comida o sexo (con la repetición cesa el mecanismo de recompensa), con la marihuana se evita este cese, lo que explica los comportamientos de consumo compulsivos.
- Abstinencia y efectos negativos: Cuando aparece la adicción, el sistema de recompensa y motivación se reorienta hacia lo que más libera DA, es decir la sustancia a la que se es adicto dejando de lado todas las otras cosas que liberan DA en menor cantidad. Adicionalmente la liberación repetida de DA en el circuito de recompensa, específicamente en el núcleo acumbens y la porción dorsal del estriado, disminuye la capacidad de producir la euforia que se obtuvo con los primeros consumos y la descarga continua afecta a la amígdala, lo que hace a los pacientes más propensos al estrés y la aparición de emociones negativas; una especie de sistema antirrecompensa.
Este sistema antirrecompensa hiperactivo hace que los pacientes experimenten disforia lo cual suma que además de consumir por los cambios en el sistema de recompensa, también se consume para evitar los síntomas negativos que aparecen cuando hay abstinencia (no pueden dejar de consumirla y consumirla ya no genera el mismo placer). - Preocupación y anticipación: En esta fase aparecen alteraciones en la función ejecutiva secundarias a cambios en la corteza prefrontal (disfunción de DA y Glutamato), afectándose la capacidad de autorregulación, toma de decisiones, selección e inicio de acción, atribución de la importancia y supervisión del error. Todo esto trae como consecuencia el empeoramiento en la capacidad de resistir los deseos de consumo.
Los factores que aumentan el riesgo de adicción son los antecedentes familiares (genéticos y pautas de crianza), exposición temprana al consumo, a ambientes de alto riesgo, fácil acceso a las drogas y ciertas patologías mentales como trastornos del estado del ánimo, TDAH, ansiedad y psicosis.
Se han realizado muchos estudios tratando de establecer un vínculo robusto entre el consumo de marihuana y la aparición de enfermedades psiquiátricas. Hasta ahora los que más estudios tienen son:
- A corto plazo: alteración de la memoria a corto plazo, coordinación motora, juicio y psicosis.
- A largo plazo: adicción, desarrollo cerebral alterado (menos fibras en precúneo, centro integrador, en la fimbria del hipocampo, importante para aprendizaje y memoria, alteraciones a nivel de las redes pre frontal, necesaria para la función ejecutiva, y subcortical, necesaria para procesar hábitos y rutinas), disminución del IQ, bronquitis crónica con mayor riesgo de neumonía y finalmente enfermedad mental (ansiedad, depresión y psicosis).
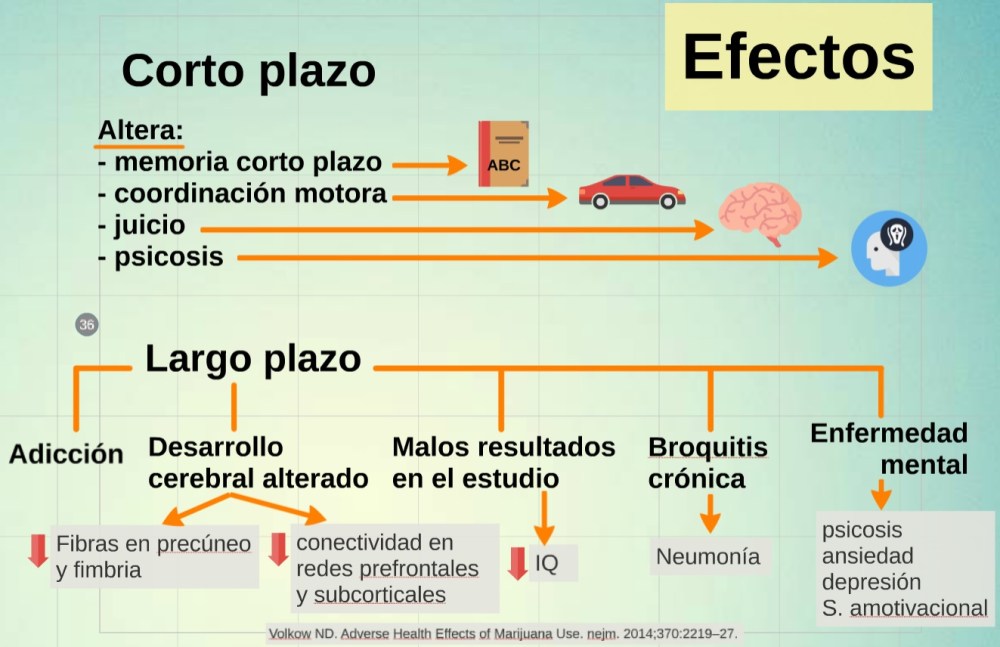
Alteraciones estructurales y funcionales a nivel cerebral
Síndrome amotivacional
Se duda de su existencia. Es una condición que aparece luego del consumo crónico de marihuana, consistente en apatía, abandono del autocuidado, indiferencia, bradicinesia, desinterés, disminución del deseo sexual; lo que conlleva a una disfunción cognitiva, social a interpersonal.
¿Por qué se duda? Solo se empezó a reportar desde la década de los 60’s (Smith, 1968), los datos científicos son escasos, antiguos y de estudios sin mucho rigor epidemiológico, se presenta en la adolescencia donde hay grandes cambios en la personalidad por lo que algunos autores plantean que el trastorno haga parte de este espectro y no tiene código diagnóstico especifico en ningún sistema de clasificación.
Otros autores plantean la posibilidad de que correspondan a los síntomas negativos de la esquizofrenia.
Alteraciones del sueño
Cuando se utiliza por un tiempo corto, la marihuana puede resolver las dificultades para conciliar el sueño. Con el uso crónico puede producir efectos negativos sobre el sueño que se intensifican en la fase de abstinencia (32-70%), como sueños extraños (1 a 3 días luego de suspender consumo), insomnio y pobre calidad del sueño (inicio entre 2 y 6 días de abstinencia y dura hasta 43 días). Puede ocurrir una situación en la que los pacientes con dependencia consumen marihuana para disminuir el insomnio; requieren dosis más altas por lo que empeoran los efectos adversos sobre el sueño, cerrando el círculo repetitivo. La mayoría de estudios tenían como criterio el uso de marihuana al menos 5 veces/semana durante los últimos 3 meses.
Mediante polisomnografía se evidencia aumento en la latencia del sueño y múltiples despertares. En las fases iniciales de la abstinencia, el sueño REM aumenta y posteriormente disminuye si la abstinencia se mantiene. El tratamiento tiene pocos estudios, pero ha mostrado efectividad los agonistas alfa 2 y la nabilona, un análogo sintético del THC. Hay otros estudios con zolpidem, mirtazapina, gabapentina y quetiapina, pero no son concluyentes.
A su vez, las alteraciones del sueño duplican el riesgo de iniciar el consumo de marihuana por los efectos descritos previamente.
Alteraciones en el embarazo
Se asocia el consumo durante el embarazo a parto pretérmino, bajo peso al nacer, feto pequeño para la edad gestacional y necesidad de ingreso a UCI neonatal. Adicionalmente, estudios de seguimiento de hijos expuestos a cannabis in útero presentan a lo largo del neurodesarrollo una mayor incidencia de fallas de la atención, función ejecutiva, menos logros académicos y más problemas del comportamiento.
El sistema endocannabinoide se expresa en el SNC a partir de la semana 16, por ende el consumo de la madre (el THC atraviesa barrera placentaria) puede interactuar y producir cambios. Además, la mayoría de estudios de teratogenicidad fueron realizados en la década de los 90, donde el promedio de THC en la marihuana consumida era de 4%, ahora el promedio es de 12%. Algunas mujeres utilizan la marihuana e incluso los medicamentos a base de cannabinoides como tratamiento antinauseoso durante el embarazo o como manejo de la hiperémesis gravídica.
5. ¿Uso terapéutico?
En el momento solo dos medicamentos a base de THC, el Marinol® (dronabinol) y el Cesamet® (Nabilone) tienen aprobación FDA para náuseas en pacientes con quimioterapia y para estimular el apetito en pacientes con síndrome de emaciación por VIH, respectivamente.
En Colombia, solo se comercializa el Sativex®. (THC 2.7mg : CBD 2.5mg / 100uL, un cigarrillo de marihuana que contenga 3.5% de THC logra en 10 minutos, concentraciones en sangre de 180ng/mL) un spray nasal utilizado en los pacientes con esclerosis múltiple que tienen espasticidad refractaria.
Bibliografía
- Revisión UNA, Sobre H, Del LOSU, Su CY. AN HISTORICAL REVIEW AMONG CANNABIS. 2006;6:47–70.
- Volkow DND. La marihuana.
- Degenhardt L, Hall W. Addiction 1 Extent of illicit drug use and dependence , and their contribution to the global burden of disease. Lancet. Elsevier Ltd; 2012;379(9810):55–70.
- Piscitelli F, Marzo V Di. The ever-expanding world of the endocannabinoids : A concise introduction. Cannabinoids in Neurologic and Mental Disease. Elsevier Inc.; 1997. xxv-xlv.
- Michael AP. The effects of Δ 9 -tetrahydrocannabinol on the dopamine system. Nat Publ Gr. Nature Publishing Group; 2016;539(7629):369–77.
- Volkow ND. Adverse Health Effects of Marijuana Use. nejm. 2014;370:2219–27.
- Article R. Neurobiologic Advances from the Brain Disease Model of Addiction. 2016;363–71.
- Macdonald K, Macdonald KAI, Pappas K, Weil A. WHY NOT POT ? A Review of the Brain- based Risks of Cannabis. 2016;13(3):13–22.
- Caspi A, Moffitt TE, Cannon M, Mcclay J, Murray R, Harrington H, et al. Moderation of the Effect of Adolescent-Onset Cannabis Use on Adult Psychosis by a Functional Polymorphism in the Catechol-O-Methyltransferase Gene : Longitudinal Evidence of a Gene X Environment Interaction. 2005;1117–27.
- Fusar-poli P, Crippa JA, Batalla A, Bhattacharyya S, Yu M. Structural and Functional Imaging Studies in Chronic Cannabis Users : A Systematic Review of Adolescent and Adult Findings. 2013;8(2).
- Angarita GA, Emadi N, Hodges S, Morgan PT. Sleep abnormalities associated with alcohol , cannabis , cocaine , and opiate use : a comprehensive review. Addict Sci Clin Pract. BioMed Central; 2016;1–17.
- Forray A, Haven N. Substance use during pregnancy [ version 1 ; referees : 2 approved ] Referee Status : 2016;5(May):1–9.
- Volkow ND. The Risks of Marijuana Use During Pregnancy. 2016;9591.
